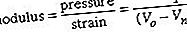elektrolyse, prosess der elektrisk strøm føres gjennom et stoff for å utføre en kjemisk endring. Den kjemiske endringen er stoffet der stoffet mister eller får et elektron (oksidasjon eller reduksjon). Prosessen utføres i en elektrolytisk celle, et apparat bestående av positive og negative elektroder som holdes fra hverandre og dyppet i en løsning som inneholder positivt og negativt ladede ioner. Stoffet som skal transformeres kan danne elektroden, kan utgjøre løsningen eller kan oppløses i løsningen. Elektrisk strøm (dvs. elektroner) kommer inn gjennom den negativt ladede elektroden (katoden); komponenter i løsningen beveger seg til denne elektroden, kombineres med elektronene og transformeres (reduseres). Produktene kan være nøytrale elementer eller nye molekyler. Komponenter av løsningen beveger seg også til den andre elektroden (anoden), gir opp sine elektroner og blir transformert (oksidert) til nøytrale elementer eller nye molekyler. Hvis stoffet som skal transformeres er elektroden, er reaksjonen ofte en der elektroden løses opp ved å gi opp elektroner.

kjemisk industri: Elektrolytisk prosess
Senere på 1800-tallet muliggjorde utviklingen av elektrisk kraftproduksjon elektrokjemisk industri. Dette er ikke tydelig identifiserbart
Elektrolyse brukes i utstrakt grad i metallurgiske prosesser, for eksempel i ekstraksjon (elektrowinning) eller rensing (elektrorfinering) av metaller fra malmer eller forbindelser og i avsetting av metaller fra løsning (elektroplettering). Metallisk natrium- og klorgass produseres ved elektrolyse av smeltet natriumklorid; elektrolyse av en vandig oppløsning av natriumklorid gir natriumhydroksyd og klorgass. Hydrogen og oksygen produseres ved elektrolyse av vann.