Oksysyre, hvilken som helst oksygenholdig syre. De fleste kovalente ikke-metalliske oksider reagerer med vann for å danne sure oksider; det vil si, de reagerer med vann og danner oksysyrer som utbytte hydroniumioner (H 3 O +) i oppløsning. Det er noen unntak, for eksempel karbonmonoksyd, CO, dinitrogenoksid, N 2 O, og nitrogenoksyd, NO.
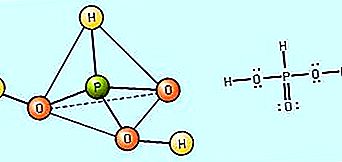
Styrken til et oksysyre er definert av i hvilken grad det dissosieres i vann (dvs. dens evne til å danne H + -ioner). Generelt kan den relative styrken til oksysyrer forutsies på grunnlag av elektronegativiteten og oksidasjonsnummeret til det sentrale ikke-metale atom. Syrestyrken øker når elektronegativiteten til sentralatomet øker. For eksempel, fordi elektronegativiteten til klor (Cl) er større enn svovel (S), som igjen er større enn fosfor (P), kan det forutsies at perklorsyre, HClO 4, er en sterkere syre enn svovelsyre, H 2 SO 4, som skal være en sterkere syre enn fosforsyre, H 3 PO 4. For et gitt ikke-metallisk sentralt atom øker syrestyrken etter hvert som oksidasjonstallet til sentralatomet øker. For eksempel er salpetersyre, HNO 3, der nitrogen (N) -atom har et oksidasjonsnummer på +5, en sterkere syre enn salpetersyre, HNO 2, hvor nitrogenoksidasjonstilstanden er +3. På samme måte, svovelsyre, H- 2 SO 4, med svovel i sin oksidasjonstilstand +6, er en sterkere syre enn svovelsyrling, H 2 SO 3, hvor en 4 oksidasjonstall av svovel eksisterer.
Saltet av en oksysyre er en forbindelse som dannes når syren reagerer med en base: syre + base → salt + vann. Denne typen reaksjoner kalles nøytralisering, fordi løsningen gjøres nøytral.













