effusjon
Vurder systemet beskrevet ovenfor i beregningen av gasstrykk, men med området A i beholderveggen erstattet med et lite hull. Antallet molekyler som slipper ut gjennom hullet i tid t er lik (1/2) (N / V) v z (At). I dette tilfellet er kollisjoner mellom molekyler betydelige, og resultatet gjelder bare for bittesmå hull i veldig tynne vegger (sammenlignet med den gjennomsnittlige frie banen), slik at et molekyl som nærmer seg hullet vil komme gjennom uten å kollidere med et annet molekyl og bli avledet bort. Forholdet mellom v z og gjennomsnittshastigheten v̄ er ganske grei: v z = (1/2) v̄.
Hvis hastighetene for to forskjellige gasser som strømmer gjennom det samme hullet sammenlignes, starter med den samme gasstettheten hver gang, blir det funnet at mye mer lett gass slipper ut enn tung gass, og at mer gass slipper ut ved en høy temperatur enn ved en lav temperatur, andre ting er like. Spesielt,
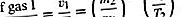
Det siste trinnet følger av energiformelen, (1/2) mv 2 = (3/2) kT, hvor (v 2) 1/2 er tilnærmet til å være v, selv om v 2 og (v̄) 2 faktisk skiller seg fra en numerisk faktor i nærheten av enhet (nemlig 3π / 8). Dette resultatet ble oppdaget eksperimentelt i 1846 av Graham for konstant temperatur og er kjent som Grahams lov om utbredelse. Den kan brukes til å måle molekylvekter, for å måle damptrykket til et materiale med et lavt damptrykk, eller til å beregne fordampningshastigheten for molekyler fra en væske eller fast overflate.
Termisk transpirasjon
Anta at to beholdere med samme gass, men ved forskjellige temperaturer, er forbundet med et lite hull og at gassen bringes til jevn tilstand. Hvis hullet er lite nok og gasstettheten er lav nok til at bare effusjon skjer, vil likevektstrykket være større på høgtemperatursiden. Men hvis starttrykkene på begge sider er like, vil gass strømme fra lavtemperatursiden til høgtemperatursiden for å føre til at høytemperaturtrykket øker. Den sistnevnte situasjonen kalles termisk transpirasjon, og stabilitetsresultatet kalles den termomolekylære trykkforskjellen. Disse resultatene følger ganske enkelt fra effusjonsformelen hvis den ideelle gassloven brukes til å erstatte N / V med p / T;
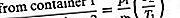
Når en stabil tilstand er nådd, er effusjonshastighetene like, og dermed
Dette fenomenet ble først undersøkt eksperimentelt av Osborne Reynolds i 1879 i Manchester, Eng. Feil kan oppstå hvis et gasstrykk blir målt i et fartøy ved veldig lav eller veldig høy temperatur ved å koble det via et fint rør til et manometer ved romtemperatur. En kontinuerlig sirkulasjon av gass kan produseres ved å forbinde de to beholderne med et annet rør hvis diameter er stor sammenlignet med den gjennomsnittlige frie vei. Trykkforskjellen driver gass gjennom dette røret ved viskøs strømning. En varmemotor basert på denne sirkulasjonsstrømmen har dessverre lav virkningsgrad.