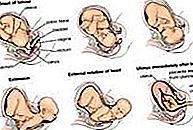
Ramaneffekt, endring i bølgelengden til lys som oppstår når en lysstråle avbøyes av molekyler. Når en lysstråle krysser en støvfri, gjennomsiktig prøve av en kjemisk forbindelse, kommer en liten brøkdel av lyset frem i andre retninger enn for den innfallende (innkommende) strålen. Det meste av dette spredte lyset har uendret bølgelengde. En liten del har imidlertid bølgelengder som er forskjellige fra det innfallende lyset; dens tilstedeværelse er et resultat av Raman-effekten.
Fenomenet er oppkalt etter den indiske fysikeren Sir Chandrasekhara Venkata Raman, som først publiserte observasjoner av effekten i 1928. (Østerriksk fysiker Adolf Smekal beskrev teoretisk effekten i 1923. Den ble først observert bare en uke før Raman av russiske fysikere Leonid Mandelstam og Grigory Landsberg; de publiserte imidlertid ikke resultatene før måneder etter Raman.)
Ramanspredning er kanskje lettest forståelig hvis det innfallende lyset anses å bestå av partikler, eller fotoner (med energi som er proporsjonal med frekvens), som treffer molekylene i prøven. De fleste av møtene er elastiske, og fotonene er spredt med uendret energi og frekvens. Noen ganger tar imidlertid molekylet opp energi fra eller gir opp energi til fotonene, som derved blir spredt med redusert eller økt energi, derav med lavere eller høyere frekvens. Frekvensforskyvningene er således målinger av energimengdene som er involvert i overgangen mellom start- og slutttilstander for spredningsmolekylet.
Raman-effekten er svak; for en flytende forbindelse kan intensiteten av det berørte lyset bare være 1/100 000 av den innfallende strålen. Mønsteret av Raman-linjene er karakteristisk for den spesielle molekylære arten, og dens intensitet er proporsjonal med antallet spredende molekyler i lysets vei. Dermed brukes Raman-spektre i kvalitativ og kvantitativ analyse.
Energiene som tilsvarer Raman-frekvensforskyvningene, er funnet å være energiene assosiert med overganger mellom forskjellige rotasjons- og vibrasjonstilstander i spredningsmolekylet. Rene rotasjonsskift er små og vanskelige å observere, bortsett fra for enkle gassformede molekyler. I væsker hindres rotasjonsbevegelser, og diskrete Raman-linjer er ikke funnet. Det meste av Raman-arbeidet er opptatt av vibrasjonsoverganger, som gir større skift som kan observeres for gasser, væsker og faste stoffer. Gasser har lav molekylkonsentrasjon ved vanlige trykk og gir derfor svært svake Raman-effekter; væsker og faste stoffer studeres derfor oftere.











![Slaget ved Kandahar andre anglo-afghanske krig [1880] Slaget ved Kandahar andre anglo-afghanske krig [1880]](https://images.thetopknowledge.com/img/world-history/6/battle-kandahar-second-anglo-afghan-war-1880.jpg)