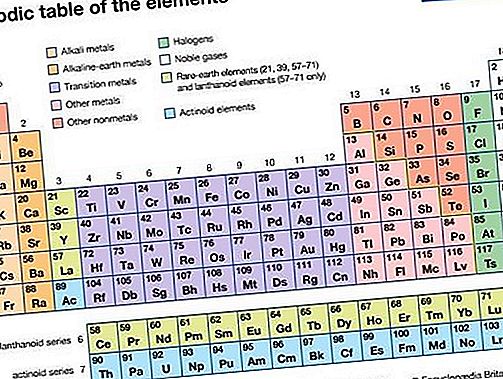
Edel gass, noen av de syv kjemiske elementene som utgjør gruppe 18 (VIIIa) i det periodiske systemet. Elementene er helium (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe), radon (Rn) og oganesson (Og). Edelgassene er fargeløse, luktfrie, smakløse, ikke brennbare gasser. De har tradisjonelt blitt merket gruppe 0 i den periodiske tabellen fordi det i flere tiår etter oppdagelsen ble antatt at de ikke kunne binde seg til andre atomer; det vil si at atomene deres ikke kunne kombinere med de fra andre elementer for å danne kjemiske forbindelser. Deres elektroniske strukturer og funnet at noen av dem faktisk danner forbindelser har ført til den mer passende betegnelsen, gruppe 18.
Da medlemmene i gruppen ble oppdaget og identifisert, ble de antatt å være svært sjeldne, så vel som kjemisk inerte, og ble derfor kalt de sjeldne eller inerte gassene. Det er imidlertid kjent at flere av disse elementene er ganske rik på Jorden og i resten av universet, så betegnelsen sjelden er misvisende. Tilsvarende har bruk av begrepet inert den ulempen at det binder kjemisk passivitet, noe som antyder at forbindelser i gruppe 18 ikke kan dannes. I kjemi og alkymi har ordet edel lenge betegnet motviljen fra metaller, som gull og platina, til å gjennomgå kjemisk reaksjon; det gjelder i samme forstand for gruppen av gasser som dekkes her.
Forekomsten av edle gasser avtar når atomantallet øker. Helium er det mest rikholdige elementet i universet bortsett fra hydrogen. Alle edle gasser er til stede i jordas atmosfære, og bortsett fra helium og radon, er deres viktigste kommersielle kilde luften, hvorfra de er oppnådd ved flytning og fraksjonert destillasjon. Det meste helium produseres kommersielt fra visse naturgassbrønner. Radon isoleres vanligvis som et produkt av radioaktiv nedbrytning av radiumforbindelser. Kjernene i radiumatomer forfaller spontant ved å avgi energi og partikler, heliumkjerner (alfapartikler) og radonatomer. Noen egenskaper for edle gasser er listet opp i tabellen.
Noen egenskaper ved edle gasser
| helium | neon | argon | krypton | xenon | radon | ununoctium | |
|---|---|---|---|---|---|---|---|
| * Kl. 25.05 atmosfærer. | |||||||
| ** hcp = sekskantet tettpakket, fcc = ansiktssentrert kubikk (kubikk tettpakket). | |||||||
| *** Stablest isotop. | |||||||
| atomnummer | 2 | 10 | 18 | 36 | 54 | 86 | 118 |
| atomvekt | 4,003 | 20.18 | 39,948 | 83,8 | 131,293 | 222 | 294 *** |
| smeltepunkt (° C) | -272,2 * | -248,59 | -189,3 | -157,36 | -111,7 | -71 | - |
| kokepunkt (° C) | -268,93 | -246,08 | -185,8 | -153,22 | -108 | -61,7 | - |
| tetthet ved 0 ° C, 1 atmosfære (gram per liter) | 0,17847 | 0,899 | 1,784 | 3,75 | 5,881 | 9,73 | - |
| løselighet i vann ved 20 ° C (kubikkcentimeter gass per 1000 gram vann) | 8,61 | 10.5 | 33.6 | 59.4 | 108,1 | 230 | - |
| isotopisk overflod (landlig, prosent) | 3 (0,000137), 4 (99,999863) | 20 (90,48), 21 (0,27), 22 (9,25) | 36 (0,3365), 40 (99,6003) | 78 (0,35), 80 (2,28), 82 (11,58), 83 (11,49), 84 (57), 86 (17,3) | 124 (0,09), 126 (0,09), 128 (1,92), 129 (26,44), 130 (4,08), 131 (21,18), 132 (26,89), 134 (10,44), 136 (8,87) | - | - |
| radioaktive isotoper (massetall) | 5-10 | 16–19, 23–34 | 30–35, 37, 39, 41–53 | 69–77, 79, 81, 85, 87–100 | 110–125, 127, 133, 135–147 | 195-228 | 294 |
| farge på lys som sendes ut av gassformig utløpsrør | gul | rød | rød eller blå | gul-grønn | blå til grønn | - | - |
| fusjonsvarme (kilojoules per mol) | 0,02 | 0,34 | 1,18 | 1,64 | 2.3 | 3 | - |
| fordampingsvarme (kalorier per mol) | 0,083 | 1,75 | 6.5 | 9.02 | 12.64 | 17 | - |
| spesifikk varme (joule per gram Kelvin) | 5,1931 | 1,03 | 0,52033 | 0,24805 | 0,15832 | 0,09365 | - |
| kritisk temperatur (K) | 5,19 | 44.4 | 150,87 | 209,41 | 289,77 | 377 | - |
| kritisk trykk (atmosfærer) | 2,24 | 27.2 | 48.34 | 54.3 | 57,65 | 62 | - |
| kritisk tetthet (gram per kubikkcentimeter) | 0,0696 | 0,4819 | 0,5356 | 0,9092 | 1,103 | - | - |
| varmeledningsevne (watt per meter Kelvin) | 0,1513 | 0,0491 | 0,0177 | 0,0094 | 0,0057 | 0,0036 | - |
| magnetisk følsomhet (cgs enheter per mol) | -,0000019 | -,0000072 | -,0000194 | -,000028 | -,000043 | - | - |
| krystallstruktur ** | hcp | fcc | fcc | fcc | fcc | fcc | - |
| radius: atomic (angstroms) | 0,31 | 0,38 | 0,71 | 0,88 | 1,08 | 1.2 | - |
| radius: kovalent (krystall) estimert (angstroms) | 0,32 | 0,69 | 0,97 | 1.1 | 1.3 | 1,45 | - |
| statisk polarisering (kubiske angstromer) | 0,204 | 0,392 | 1,63 | 2,465 | 4,01 | - | - |
| ioniseringspotensial (først elektron volt) | 24,587 | 21,565 | 15,759 | 13,999 | 12,129 | 10,747 | - |
| elektronegativitet (Pauling) | 4.5 | 4.0 | 2.9 | 2.6 | 2,25 | 2.0 | - |











