Anhydrid, hvilken som helst kjemisk forbindelse oppnådd, enten i praksis eller i prinsippet, ved eliminering av vann fra en annen forbindelse. Eksempler på uorganiske anhydrider er svoveltrioksyd, SO 3, som er avledet fra svovelsyre, og kalsiumoksyd, CaO, avledet fra kalsiumhydroksyd. Svoveltrioksyd og andre oksider dannet ved fjerning av vann fra en syre kalles ofte syreanhydrider, mens de som kalsiumoksyd som produseres av en base ved tap av vann, er betegnet som basiske anhydrider.
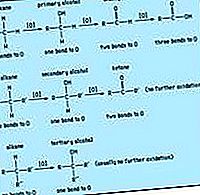
karboksylsyre: Anhydrider
Den funksjonelle gruppen av et karboksylsyreanhydrid er to acylgrupper bundet til et oksygenatom. Anhydriden kan være symmetrisk (to identiske
Den viktigste av de organiske anhydrider er eddiksyreanhydrid, (CH 3 CO) 2 O. Det fremstilles industrielt på en av to måter: ved atmosfærisk oksydasjon av acetaldehyd i nærvær av et metall-acetat; og fra eddiksyre ved omsetning med acetylen eller keten. Andre organiske anhydrider kan fremstilles fra karboksylsyrer ved omsetning med eddiksyreanhydrid, keten, metoksyacetylen eller isopropenylacetat. Anhydrider produseres også når acylhalogenider reagerer med eddiksyreanhydrid eller med karboksylsyre og pyridin.
De organiske anhydridene brukes til å introdusere acylgruppen (RCO) i organisk syntese. De reagerer med vann for å gi karboksylsyrer, med alkoholer eller fenoler for å gi estere, og med ammoniakk og aminer for å gi amider. Eddiksyreanhydrid anvendes ved fremstilling av celluloseacetat, som er mye brukt som base for magnetbånd og til fremstilling av tekstilfibre. Den blir også oppvarmet med salisylsyre for å produsere den medisinsk kjemiske acetylsalisylsyre (aspirin).